Подготовка выпускников к ЕГЭ. "Тема электролиза в ЕГЭ"
Что такое электролиз? Для более простого понимания ответа на этот вопрос давайте представим себе любой источник постоянного тока. У каждого источника постоянного тока всегда можно найти положительный и отрицательный полюс:
Подсоединим к нему две химически стойких электропроводящих пластины, которые назовем электродами. Пластину, присоединенную к положительному полюсу назовем анодом, а к отрицательному катодом:
Хлорид натрия является электролитом, при его расплавлении происходит диссоциация на катионы натрия и хлорид-ионы:
NaCl = Na + + Cl −
Очевидно, что заряженные отрицательно анионы хлора направятся к положительно заряженному электроду – аноду, а положительно заряженные катионы Na + направятся к отрицательно заряженному электроду – катоду. В результате этого и катионы Na + и анионы Cl − разрядятся, то есть станут нейтральными атомами. Разрядка происходит посредством приобретения электронов в случае ионов Na + и потери электронов в случае ионов Cl − . То есть на катоде протекает процесс:
Na + + 1e − = Na 0 ,
А на аноде:
Cl − − 1e − = Cl
Поскольку каждый атом хлора имеет по неспаренному электрону, одиночное существование их невыгодно и атомы хлора объединяются в молекулу из двух атомов хлора:
Сl∙ + ∙Cl = Cl 2
Таким образом, суммарно, процесс, протекающий на аноде, правильнее записать так:
2Cl − − 2e − = Cl 2
То есть мы имеем:
Катод: Na + + 1e − = Na 0
Анод: 2Cl − − 2e − = Cl 2
Подведем электронный баланс:
Na + + 1e − = Na 0 |∙2
2Cl − − 2e − = Cl 2 |∙1<
Сложим левые и правые части обоих уравнений полуреакций , получим:
2Na + + 2e − + 2Cl − − 2e − = 2Na 0 + Cl 2
Сократим два электрона аналогично тому, как это делается в алгебре получим ионное уравнение электролиза:
2NaCl (ж.) => 2Na + Cl 2
Рассмотренный выше случай является с теоретической точки зрения наиболее простым, поскольку в расплаве хлорида натрия из положительно заряженных ионов были только ионы натрия, а из отрицательных – только анионы хлора.
Другими словами, ни у катионов Na + , ни у анионов Cl − не было «конкурентов» за катод и анод.
А, что будет, например, если вместо расплава хлорида натрия ток пропустить через его водный раствор? Диссоциация хлорида натрия наблюдается и в этом случае, но становится невозможным образование металлического натрия в водном растворе. Ведь мы знаем, что натрий – представитель щелочных металлов – крайне активный металл, реагирующий с водой очень бурно. Если натрий не способен восстановиться в таких условиях, что же тогда будет восстанавливаться на катоде?
Давайте вспомним строение молекулы воды. Она представляет собой диполь, то есть у нее есть отрицательный и положительный полюсы:
Именно благодаря этому свойству, она способна «облеплять» как поверхность катода, так и поверхность анода:
При этом могут происходить процессы:
2H 2 O + 2e − = 2OH − + H 2
2H 2 O – 4e − = O 2 + 4H +
Таким образом, получается, что если мы рассмотрим раствор любого электролита, то мы увидим, что катионы и анионы, образующиеся при диссоциации электролита, конкурируют с молекулами воды за восстановление на катоде и окисление на аноде.
Так какие же процессы будут происходить на катоде и на аноде? Разрядка ионов, образовавшихся при диссоциации электролита или окисление/восстановление молекул воды? Или, возможно, будут происходить все указанные процессы одновременно?
В зависимости от типа электролита при электролизе его водного раствора возможны самые разные ситуации. Например, катионы щелочных, щелочноземельных металлов, алюминия и магния просто не способны восстановиться в водной среде, так как при их восстановлении должны были бы получаться соответственно щелочные, щелочноземельные металлы, алюминий или магний т.е. металлы, реагирующие с водой.
В таком случае является возможным только восстановление молекул воды на катоде.
Запомнить то, какой процесс будет протекать на катоде при электролизе раствора какого-либо электролита можно, следуя следующим принципам:
1) Если электролит состоит из катиона металла, который в свободном состоянии в обычных условиях реагирует с водой, на катоде идет процесс:
2H 2 O + 2e − = 2OH − + H 2
Это касается металлов, находящихся в начале ряда активности по Al включительно.
2) Если электролит состоит из катиона металла, который в свободном виде не реагирует с водой, но реагирует с кислотами неокислителями, идут сразу два процесса, как восстановления катионов металла, так и молекул воды:
Me n+ + ne = Me 0
К таким металлам относятся металлы, находящиеся между Al и Н в ряду активности.
3) Если электролит состоит из катионов водорода (кислота) или катионов металлов, не реагирующих с кислотами неокислителями — восстанавливаются только катионы электролита:
2Н + + 2е − = Н 2 – в случае кислоты
Me n + + ne = Me 0 – в случае соли
На аноде тем временем ситуация следующая:
1) Если электролит содержит анионы бескислородных кислотных остатков (кроме F −), то на аноде идет процесс их окисления, молекулы воды не окисляются. Например:
2Сl − − 2e = Cl 2
S 2- − 2e = S o
Фторид-ионы не окисляются на аноде поскольку фтор не способен образоваться в водном растворе (реагирует с водой)
2) Если в состав электролита входят гидроксид-ионы (щелочи) они окисляются вместо молекул воды:
4ОН − − 4е − = 2H 2 O + O 2
3) В случае того, если электролит содержит кислородсодержащий кислотный остаток (кроме остатков органических кислот) или фторид-ион (F −) на аноде идет процесс окисления молекул воды:
2H 2 O – 4e − = O 2 + 4H +
4) В случае кислотного остатка карбоновой кислоты на аноде идет процесс:
2RCOO − − 2e − = R-R + 2CO 2
Давайте потренируемся записывать уравнения электролиза для различных ситуаций:
Пример №1
Напишите уравнения процессов протекающих на катоде и аноде при электролизе расплава хлорида цинка, а также общее уравнение электролиза.
Решение
При расплавлении хлорида цинка происходит его диссоциация:
ZnCl 2 = Zn 2+ + 2Cl −
Далее следует обратить внимание на то, что электролизу подвергается именно расплав хлорида цинка, а не водный раствор. Другими словами, без вариантов, на катоде может происходить только восстановление катионов цинка, а на аноде окисление хлорид-ионов т.к. отсутствуют молекулы воды:
Катод: Zn 2+ + 2e − = Zn 0 |∙1
Анод: 2Cl − − 2e − = Cl 2 |∙1
ZnCl 2 = Zn + Cl 2
Пример №2
Напишите уравнения процессов протекающих на катоде и аноде при электролизе водного раствора хлорида цинка, а также общее уравнение электролиза.
Так как в данном случае, электролизу подвергается водный раствор, то в электролизе, теоретически, могут принимать участие молекулы воды. Так как цинк расположен в ряду активности между Al и Н то это значит, что на катоде будет происходить как восстановление катионов цинка, так и молекул воды.
2H 2 O + 2e − = 2OH − + H 2
Zn 2+ + 2e − = Zn 0
Хлорид-ион является кислотным остатком бескислородной кислоты HCl, поэтому в конкуренции за окисление на аноде хлорид-ионы «выигрывают» у молекул воды:
2Cl − − 2e − = Cl 2
В данном конкретном случае нельзя записать суммарное уравнение электролиза, поскольку неизвестно соотношение между выделяющимися на катоде водородом и цинком.
Пример №3
Напишите уравнения процессов протекающих на катоде и аноде при электролизе водного раствора нитрата меди, а также общее уравнение электролиза.
Нитрат меди в растворе находится в продиссоциированном состоянии:
Cu(NO 3) 2 = Cu 2+ + 2NO 3 −
Медь находится в ряду активности правее водорода, то есть на катоде восстанавливаться будут катионы меди:
Cu 2+ + 2e − = Cu 0
Нитрат-ион NO 3 − — кислородсодержащий кислотный остаток, это значит, что в окислении на аноде нитрат ионы «проигрывают» в конкуренции молекулам воды:
2H 2 O – 4e − = O 2 + 4H +
Таким образом:
Катод: Cu 2+ + 2e − = Cu 0 |∙2
2Cu 2+ + 2H 2 O = 2Cu 0 + O 2 + 4H +
Полученное в результате сложения уравнение является ионным уравнением электролиза. Чтобы получить полное молекулярное уравнение электролиза нужно добавить по 4 нитрат иона в левую и правую часть полученного ионного уравнения в качестве противоионов. Тогда мы получим:
2Cu(NO 3) 2 + 2H 2 O = 2Cu 0 + O 2 + 4HNO 3
Пример №4
Напишите уравнения процессов, протекающих на катоде и аноде при электролизе водного раствора ацетата калия, а также общее уравнение электролиза.
Решение:
Ацетат калия в водном растворе диссоциирует на катионы калия и ацетат-ионы:
СН 3 СООК = СН 3 СОО − + К +
Калий является щелочным металлом, т.е. находится в ряду электрохимическом ряду напряжений в самом начале. Это значит, что его катионы не способны разряжаться на катоде. Вместо них восстанавливаться будут молекулы воды:
2H 2 O + 2e − = 2OH − + H 2
Как уже было сказано выше, кислотные остатки карбоновых кислот «выигрывают» в конкуренции за окисление у молекул воды на аноде:
2СН 3 СОО − − 2e − = CH 3 −CH 3 + 2CO 2
Таким образом, подведя электронный баланс и сложив два уравнения полуреакций на катоде и аноде получаем:
Катод: 2H 2 O + 2e − = 2OH − + H 2 |∙1
Анод: 2СН 3 СОО − − 2e − = CH 3 −CH 3 + 2CO 2 |∙1
2H 2 O + 2СН 3 СОО − = 2OH − + Н 2 + CH 3 −CH 3 + 2CO 2
Мы получили полное уравнение электролиза в ионном виде. Добавив по два иона калия в левую и правую часть уравнения и сложив с противоионами мы получаем полное уравнение электролиза в молекулярном виде:
2H 2 O + 2СН 3 СООK = 2KOH + Н 2 + CH 3 −CH 3 + 2CO 2
Пример №5
Напишите уравнения процессов, протекающих на катоде и аноде при электролизе водного раствора серной кислоты, а также общее уравнение электролиза.
Серная кислота диссоциирует на катионы водорода и сульфат-ионы:
H 2 SO 4 = 2H + + SO 4 2-
На катоде будет происходить восстановление катионов водорода H + , а на аноде окисление молекул воды, поскольку сульфат-ионы являются кислородсодержащими кислотными остатками:
Катод: 2Н + + 2e − = H 2 |∙2
Анод: 2H 2 O – 4e − = O 2 + 4H + |∙1
4Н + + 2H 2 O = 2H 2 + O 2 + 4H +
Сократив ионы водорода в левой и правой и левой части уравнения получим уравнение электролиза водного раствора серной кислоты:
2H 2 O = 2H 2 + O 2
Как можно видеть, электролиз водного раствора серной кислоты сводится к электролизу воды.
Пример №6
Напишите уравнения процессов, протекающих на катоде и аноде при электролизе водного раствора гидроксида натрия, а также общее уравнение электролиза.
Диссоциация гидроксида натрия:
NaOH = Na + + OH −
На катоде будут восстанавливаться только молекулы воды, так как натрий – высокоактивный металл, на аноде только гидроксид-ионы:
Катод: 2H 2 O + 2e − = 2OH − + H 2 |∙2
Анод: 4OH − − 4e − = O 2 + 2H 2 O |∙1
4H 2 O + 4OH − = 4OH − + 2H 2 + O 2 + 2H 2 O
Сократим две молекулы воды слева и справа и 4 гидроксид-иона и приходим к тому, что, как и в случае серной кислоты электролиз водного раствора гидроксида натрия сводится к электролизу воды.
Электролиз (греч. elektron - янтарь + lysis - разложение) - химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их составные части под действием электрического тока.
Процесс электролиза заключается в перемещении катионов (положительно заряженных ионов) к катоду (заряжен отрицательно), и отрицательно заряженных ионов (анионов) к аноду (заряжен положительно).
Итак, анионы и катионы устремляются соответственно к аноду и катоду. Здесь и происходит химическая реакция. Чтобы успешно решать задания по этой теме и писать реакции, необходимо разделять процессы на катоде и аноде. Именно так и будет построена эта статья.
Катод
К катоду притягиваются катионы - положительно заряженные ионы: Na + , K + , Cu 2+ , Fe 3+ , Ag + и т.д.
Чтобы установить, какая реакция идет на катоде, прежде всего, нужно определиться с активностью металла: его положением в электрохимическом ряду напряжений металлов.
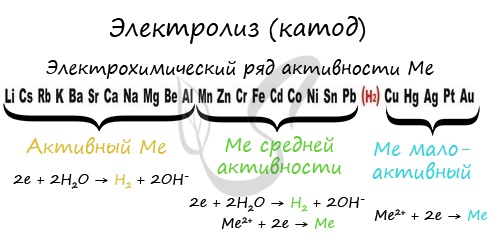
Если на катоде появился активный металл (Li, Na, K) то вместо него восстанавливаются молекулы воды, из которых выделяется водород. Если металл средней активности (Cr, Fe, Cd) - на катоде выделяется и водород, и сам металл. Малоактивные металлы выделяются на катоде в чистом виде (Cu, Ag).
Замечу, что границей между металлами активными и средней активности в ряду напряжений считается алюминий. При электролизе на катоде металлы до алюминия (включительно!) не восстанавливаются, вместо них восстанавливаются молекулы воды - выделяется водород.
В случае, если на катод поступают ионы водорода - H + (например при электролизе кислот HCl, H 2 SO 4) восстанавливается водород из молекул кислоты: 2H + - 2e = H 2
Анод
К аноду притягиваются анионы - отрицательно заряженные ионы: SO 4 2- , PO 4 3- , Cl - , Br - , I - , F - , S 2- , CH 3 COO - .

При электролизе кислородсодержащих анионов: SO 4 2- , PO 4 3- - на аноде окисляются не анионы, а молекулы воды, из которых выделяется кислород.
Бескислородные анионы окисляются и выделяют соответствующие галогены. Сульфид-ион при оксилении окислении серу. Исключением является фтор - если он попадает анод, то разряжается молекула воды и выделяется кислород. Фтор - самый электроотрицательный элемент, поэтому и является исключением.
Анионы органических кислот окисляются особым образом: радикал, примыкающий к карбоксильной группе, удваивается, а сама карбоксильная группа (COO) превращается в углекислый газ - CO 2 .
Примеры решения
В процессе тренировки вам могут попадаться металлы, которые пропущены в ряду активности. На этапе обучения вы можете пользоваться расширенным рядом активности металлов.
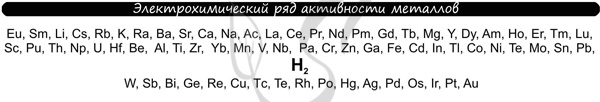
Теперь вы точно будете знать, что выделяется на катоде;-)
Итак, потренируемся. Выясним, что образуется на катоде и аноде при электролизе растворов AgCl, Cu(NO 3) 2 , AlBr 3 , NaF, FeI 2 , CH 3 COOLi.

Иногда в заданиях требуется записать реакцию электролиза. Сообщаю: если вы понимаете, что образуется на катоде, а что на аноде, то написать реакцию не составляет никакого труда. Возьмем, например, электролиз NaCl и запишем реакцию:
NaCl + H 2 O → H 2 + Cl 2 + NaOH
Натрий - активный металл, поэтому на катоде выделяется водород. Анион не содержит кислорода, выделяется галоген - хлор. Мы пишем уравнение, так что не можем заставить натрий испариться бесследно:) Натрий вступает в реакцию с водой, образуется NaOH.
Запишем реакцию электролиза для CuSO 4:
CuSO 4 + H 2 O → Cu + O 2 + H 2 SO 4
Медь относится к малоактивным металлам, поэтому сама в чистом виде выделяется на катоде. Анион кислородсодержащий, поэтому в реакции выделяется кислород. Сульфат-ион никуда не исчезает, он соединяется с водородом воды и превращается в серую кислоту.
Электролиз расплавов
Все, что мы обсуждали до этого момента, касалось электролиза растворов, где растворителем является вода.
Перед промышленной химией стоит важная задача - получить металлы (вещества) в чистом виде. Малоактивные металлы (Ag, Cu) можно легко получать методом электролиза растворов.
Но как быть с активными металлами: Na, K, Li? Ведь при электролизе их растворов они не выделяются на катоде в чистом виде, вместо них восстанавливаются молекулы воды и выделяется водород. Тут нам как раз пригодятся расплавы, которые не содержат воды.
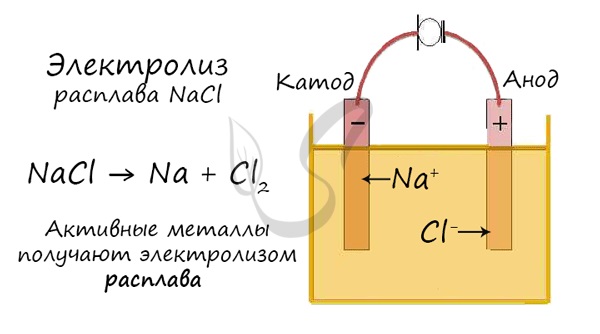
В безводных расплавах реакции записываются еще проще: вещества распадаются на составные части:
AlCl 3 → Al + Cl 2
LiBr → Li + Br 2
© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к
Тема 6. «Электролиз растворов и расплавов солей»
1. Электролиз – окислительно – восстановительный процесс, протекающий на электродах при пропускании электрического тока через раствор или расплав электролита.
2. Катод – отрицательнозаряженный электрод. Происходит восстановление катионов металлов и водорода (в кислотах) или молекул воды.
3. Анод – положительнозаряженный электрод. Происходит окисление анионов кислотного остатка и гироксогруппы (в щелочах).
4. При электролизе раствора соли в реакционной смеси присутствует вода. Поскольку вода может проявлять и окислительные и восстановительные свойства, то она является «конкурентом» и для катодных и для анодных процессов.
5. Различают электролиз с инертными электродами (графитовые, угольные, платиновые) и активным анодом (растворимым), а также электролиз расплавов и растворов электролитов.
КАТОДНЫЕ ПРОЦЕССЫ
Если металл находится в ряду напряжений:
Положение металла в ряду напряжений
Восстановление на катоде
от Li до Al
Восстанавливаются молекулы воды: 2H2O + 2e- → H20+ 2OH-
от Mn до Pb
Восстанавливаются и молекулы воды и катионы металла:
2H2O + 2e- → H20+ 2OH-
Men+ + ne- → Me0
от Сu до Au
Восстанавливаются катионы металлов: Men+ + ne- → Me0
АНОДНЫЕ ПРОЦЕССЫ
Кислотный остаток
Асm-
Анод
Растворимый
(железо, цинк, медь, серебро)
Нерастворимый
(графит, золото, платина)
Бескислородный
Окисление металла анода
М0 – nе- = Mn+
анод раствор
Окисление аниона (кроме F-)
Асm- - me- = Ас0
Кислородсодержащий
Фторид – ион (F-)
В кислотной и нейтральной средах:
2 H2O - 4e- → О20 + 4H+
В щелочной среде:
4ОН- - 4е- = О20+ 2Н2O
Примеры процессов электролиза расплавов с инертными электродами
В расплаве электролита присутствуют только его ионы, поэтому на катоде восстанавливаются катионы электролита, а на аноде окисляются анионы.
1. Рассмотрим электролиз расплава хлорида калия.
Термическая диссоциация КСl → K+ + Cl-
К(-) К+ + 1e- → K0
А (+) 2Сl- - 2e- → Cl02
Cуммарное уравнение:
2КСl → 2K0 + Cl20
2. Рассмотрим электролиз расплава хлорида кальция.
Термическая диссоциация СаСl2 → Са2+ + 2Сl-
К(-) Са2+ + 2e- → Са0
А (+) 2Сl- - 2e- → Cl02
Cуммарное уравнение:
СаСl2 → Ca0 + Cl20
3. Рассмотрим электролиз расплава гидроксида калия.
Термическая диссоциация КОН → К+ + ОН-
К(-) К+ + 1e- → К0
А (+) 4ОН- - 4e- → О20 + 2Н2О
Cуммарное уравнение:
4КОН → 4К0 + О20 + 2Н2О
Примеры процессов электролиза растворов электролитов с инертными электродами
В отличие от расплавов в растворе электролита, кроме его ионов, присутствуют молекулы воды. Поэтому при рассмотрении процессов на электродах необходимо учитывать их участие. Электролиз раствора соли, образованной активным металлом, стоящим в ряду напряжений до алюминия и кислотным остатком кислородосодержащей кислоты сводится к электролизу воды. 1. Рассмотрим электролиз водного раствора сульфата магния. MgSO4 – соль, которая образована металлом, стоящим в ряду напряжений до алюминия и кислородсодержащим кислотным остатаком. Уравнение диссоциации: MgSO4 → Mg2+ + SO42- К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2Н2О – 4е- = О20 + 4Н+ Суммарное уравнение: 6Н2О = 2Н20 + 4ОН- + О20 + 4Н+ 2Н2О = 2Н20 + О20 2. Рассмотрим электролиз водного раствора сульфата меди (II). СuSO4 – соль, котороая образована малоактивным металлом и кислородсодержащим кислотным остатком. В данном случае при электролизе получается металл, кислород, а в катодно-анодном пространстве образуется соответствующая кислота. Уравнение диссоциации: CuSO4 → Cu2+ + SO42- К (-) Cu2+ + 2e- = Cu0 А (+) 2Н2О – 4е- = О20 + 4Н+ Суммарное уравнение: 2Cu2+ + 2Н2О = 2Cu0 + О20 + 4Н+ 2CuSO4 + 2Н2О = 2Cu0 + О20 + 2Н2SO4
3. Рассмотрим электролиз водного раствора хлорида кальция. CаCl2 – соль, котороя образована активным металлом и бескислородным кислотным остатком. В данном случае при электролизе образуются водород, галоген, а в катодно – анодном пространстве образуется щелочь. Уравнение диссоциации: CаCl2 → Ca2+ + 2Cl- К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2Сl- – 2е- = Cl20 Суммарное уравнение: 2Н2О + 2Cl- = Cl20 + 2OН- CaCl2 + 2Н2О = Ca(OH)2 + Cl20 + Н20 4. Рассмотрим электролиз водного раствора хлорида меди (II). CuCl2 – соль, которая образована малоактивным металлом и кислотным остатком бескислородной кислоты. В данном случае образуются металл и галоген. Уравнение диссоциации: CuCl2 → Cu2+ + 2Cl- К (-) Cu2+ + 2e- = Cu0 А (+) 2Сl- – 2е- = Cl20 Суммарное уравнение: Cu2+ + 2Cl- = Cu0 + Cl20 CuCl2 = Cu0 + Cl20 5. Рассмотрим процесс электролиза раствора ацетата натрия. СН3СООNa – соль, которая образована активным металлом и кислотным остатком карбоновой кислоты. При электролизе получается водород, щелочь. Уравнение диссоциации: СН3СООNa → СН3СОО - + Na+ К (-) 2Н2О + 2е- = Н20 + 2ОН- А (+) 2CH3COO¯− 2e = C2H6 + 2CO2 Суммарное уравнение: 2Н2О + 2CH3COO¯ = Н20 + 2ОН - + C2H6 + 2CO2 2Н2О + 2CH3COONa = 2NaОH + Н20 + C2H6 + 2CO2 6. Рассмотрим процесс электролиза раствора нитрата никеля. Ni(NO3)2 - соль, которая образована металлом, стоящим в ряду напряжений от Mn до H2 и кислородсодержащим кислотным остатком. В процессе получаем металл, водород, кислород и кислоту. Уравнение диссоциации: Ni(NO3)2 → Ni2+ + 2NO3- К (-) Ni2+ +2e- = Ni0 2Н2О + 2е- = Н20 + 2ОН- A (+) 2H2O – 4e- = O20 + 4H+ Cуммарное уравнение: Ni2+ + 2Н2О + 2H2O = Ni0 + Н20 + 2ОН- + O20 + 4H+ Ni(NO3)2 + 2Н2О = Ni0 +2HNO3 + Н20 + O20 7. Рассмотрим процесс электролиза раствора серной кислоты. Уравнение диссоциации: H2SO4 → 2H+ + SO42- К (-) 2Н+ +2e- = Н20 A (+) 2H2O – 4e- = O20 + 4H+ Cуммарное уравнение: 2Н2О + 4Н+ = 2Н20 + O20 + 4H+ 2H2O = 2Н20 + O20
8. Рассмотрим процесс электролиза раствора гидроксида натрия. В данном случае идет только электролиз воды. Аналогично протекает электролиз растворов H2SO4, NaNO3, K2SO4 и др. Уравнение диссоциации: NaOH → Na+ + OH- К (-) 2H2O + 2e- = H20 + 2OH- A (+) 4OH- – 4e- = O20 + 2H2O Cуммарное уравнение: 4H2O + 4OH- = 2H20 + 4OH- + O20 + 2H2O 2H2O = 2H20 + O20
Примеры процессов электролиза растворов электролитов с растворимыми электродами
Растворимый анод при электролизе сам подвергается окислению (растворению). 1. Рассмотрим процесс электролиза сульфата меди (II) с медным анодом. При электролизе раствора сульфата меди с медным анодом процесс сводится к выделению меди на катоде и постепенному растворению анода, несмотря на природу аниона. Количество сульфата меди в растворе остается неизменным. Уравнение диссоциации: CuSO4 → Cu2+ + SO42- K (-) Cu2+ +2e- → Cu0 A (+) Cu0 - 2e- → Cu2+ переход ионов меди с анода на катод
Примеры заданий по данной теме в вариантах ЕГЭ
В3. (Вар.5)
Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах.
ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА
A) Al2(SO4)3 1. гидроксид металла, кислота
Б) СsOH 2. металл, галоген
В) Hg(NO3)2 3. металл, кислород
Г) AuBr3 4. водород, галоген 5. водород, кислород 6. металл, кислота, кислород Ход рассуждений: 1. При электролизе Al2(SO4)3 и СsOH на катоде идет восстановление воды до водорода. Исключаем варианты 1, 2, 3 и 6. 2. Для Al2(SO4)3 на аноде окисляется вода до кислорода. Выбираем вариант 5. Для СsOH на аноде окисляется гидроксид ион до кислорода. Выбираем вариант 5. 3. При электролизе Hg(NO3)2 и АuBr3 на катоде идёт восстановление катионов металла. 4. Для Hg(NO3)2 на аноде окисляется вода. Нитрат ионы в растворе связываются с катионами водорода, образуя в анодном пространстве азотную кислоту. Выбираем вариант 6. 5. Для АuBr3 на аноде окисляется анион Br- до Br2. Выбираем вариант 2.
А
Б
В
Г
5
5
6
2
В3. (Вар.1)
Установите соответствие между названием вещества и способом его получения.
НАЗВАНИЕ ВЕЩЕСТВА ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ А) литий 1) раствора LiF Б) фтор 2) расплава LiF В) серебро 3) раствора MgCl2 Г) магний 4) раствора AgNO3 5) расплава Ag2O 6) расплава MgCl2 Ход рассуждений: 1. Аналогично электролизу расплава хлорида натрия, протекает процесс электролиза расплава фторида лития. Для вариантов А и Б выбираем ответы 2. 2. Серебро возможно восстановить из раствора её соли – нитрата серебра. 3. Из раствора соли магний восстановить нельзя. Выбираем вариант 6 – расплав хлорида магния.
А
Б
В
Г
2
2
4
6
В3. (Вар.9)
Установите соответствие между формулой соли и уравнением процесса, протекающего на катоде при электролизе её водного раствора.
ФОРМУЛА СОЛИ УРАВНЕНИЕ КАТОДНОГО ПРОЦЕССА
А) Al(NO3)3 1) 2H2O – 4e- → O2 + 4H+
Б) CuCl2 2) 2H2O + 2e- → H2 + 2OH-
В) SbCl3 3) Cu2+ + 1e- → Cu+
Г) Cu(NO3)2 4) Sb3+ - 2 e- → Sb5+ 5) Sb3+ + 3e- → Sb0
6) Cu2+ + 2e- → Cu0
Ход рассуждений: 1. На катоде протекают процессы восстановления катионов металлов либо воды. Поэтому сразу исключаем варианты 1 и 4. 2. Для Al(NO3)3: на катоде идёт процесс восстановления воды. Выбираем вариант 2. 3. Для CuCl2: восстанавливаются катионы металла Cu2+. Выбираем вариант 6. 4. Для SbСl3: восстанавливаются катионы металла Sb3+. Выбираем вариант 5. 5. Для Cu(NO3)2: восстанавливаются катионы металла Cu2+. Выбираем вариант 6.
А
Б
В
Г
2